Puntos Clave
- La política de Estados Unidos de refuerzos anuales Covid-19 para casi todos es más agresiva que otras naciones. Su beneficio en bajo riesgo es incierto y la aceptación es baja.
- Esta estrategia y el debate han podido mermar la confianza pública en la vacunación general, afectando programas vitales como el de la vacuna contra sarampión, paperas y rubéola (MMR).
- La FDA propone actualizar pautas: mantener refuerzos para mayores de 65 y personas con factores de riesgo, pero exigir datos de ensayos clínicos para personas sanas de 6 meses a 64 años.
- Futuros ensayos para bajo riesgo evaluarán resultados clínicos (Covid sintomático/grave), eficacia >30%, incluirán placebos y seguimiento de al menos 6 meses.
- A diferencia de la gripe, la evolución del SARS-CoV-2 y la inmunidad natural sugieren que actualizaciones anuales de vacuna Covid-19 podrían no ser siempre necesarias.
- El objetivo de la FDA es equilibrar el acceso para alto riesgo con exigencia de evidencia científica sólida para bajo riesgo, forzando la generación de datos.
- Es probable que Argentina adopte estas nuevas directrices basadas en la evidencia, considerando que la aceptación del refuerzo Covid-19 fue inferior al 10% de la población objetivo.
Año tras año
En los últimos 5 años, Estados Unidos avanzó hacia un programa anual de refuerzo contra el Covid-19.
Cada otoño, se desarrollan vacunas de refuerzo contra el Covid-19, junto con las vacunas contra la influenza estacional, y se recomiendan para todos los estadounidenses, a partir de los 6 meses de vida. Estás vacunas están autorizadas ampliamente para su uso.
En comparación con las políticas de vacunación de todas las naciones europeas, Canadá y Australia, la política estadounidense ha sido la más agresiva.
En efecto, todas las demás naciones de altos ingresos limitan las recomendaciones de vacunas a los adultos mayores (normalmente los mayores de 65 años) o a aquellos con alto riesgo de padecer Covid-19 grave.
Si bien el rápido desarrollo de múltiples vacunas contra el SARS-CoV-2 en 2020 representó un importante logro científico, médico y regulatorio.
El beneficio de los refuerzos, especialmente entre personas de bajo riesgo que hayan recibido previamente múltiples dosis de vacunas contra el Covid-19, qué hayan tenido múltiples infecciones por este virus, o ambas, es incierto.
Dudas sobre refuerzos anuales y un efecto dominó con otras vacunas
Al igual que muchos profesionales de la salud, sigue sin estar convencido.
En las últimas 2 temporadas, la aceptación de la dosis anual de refuerzo contra el Covid-19 ha sido deficiente:
- < 10% de los niños menores de 12 años recibió un refuerzo en 2024-2025
- < 25% de los estadounidenses recibieron una dosis de refuerzo en 2024-2025
- 50% de los adultos mayores de 75 años recibió un refuerzo en 2024-2025
- < 33% de los trabajadores de la salud recibieron un refuerzo en 2023-2024
Además, la confianza pública en la vacunación en general disminuyó.esto generó una reticencia a vacunar que está afectando incluso a programas de inmunización vitales como el de la vacuna contra el sarampión, las paperas y la rubéola (MMR), que se ha establecido claramente como segura y altamente efectiva.
En efecto, en los últimos años, la reducción de las tasas de vacunación con MMR ha sido una preocupación creciente y ha contribuido a enfermedades graves y muertes por sarampión.
Nuevas recomendaciones en puerta
En este contexto la FDA planea actualizar su marco regulatorio de vacunación contra el Covid-19
Con base en la inmunogenicidad (prueba de que una vacuna puede generar títulos de anticuerpos en las personas), existen hallazgos favorables de beneficio-riesgo para:
- Adultos mayores de 65 años.
- Todas las personas mayores de 6 meses con uno o más factores de riesgo que las ponen en alto riesgo de resultados graves del Covid-19.
Para todas las personas sanas (aquellas sin factores de riesgo de Covid-19 grave) entre las edades de 6 meses y 64 años, la FDA anticipa la necesidad de datos de ensayos controlados aleatorios que evalúen los resultados clínicos que avalen vacunar a este grupo.
Esto difiere en parte con el consenso global de vacunar anualmente al grupo de edad de 50 a 64 años. Además, ya no recomiendan vacunar a las embarazadas, a diferencia de otros lugares del globo.
¿Cuáles son los factores de riesgo de Covid-19 graves considerados por el CDC?
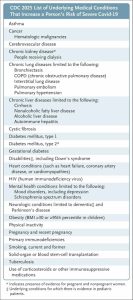
Nuevos lineamientos para futuras vacunas Covid-19
La población idel de prueba propuesta son adultos de 50 a 64 años, sin factores de riesgo.
El criterio de valoración principal preferido por la FDA en estos ensayos será el Covid-19 sintomático, con especial atención a varios criterios de valoración secundarios:
- Covid-19 grave.
- Hospitalización.
- Muerte.
Los cálculos del tamaño de la muestra deben apuntar a demostrar que las vacunas reducen la incidencia del criterio de valoración principal con un límite inferior del intervalo de confianza idealmente superior al 30 %.
No se debe excluir a las personas que hayan tenido Covid-19 en el último año, ya que se necesita evidencia para el estadounidense promedio.
El seguimiento debe extenderse por un mínimo de 6 meses para asegurar que persistan los beneficios iniciales de las dosis de refuerzo.
El grupo de control podría recibir un placebo de solución salina para permitir la documentación del perfil completo de eventos adversos.
En definitiva, estos estudios por sí solos pueden confirmar que la estrategia estadounidense de dosis de refuerzo repetidas a perpetuidad está basada en la evidencia.
¿Qué cambiaría con las nuevas recomendaciones?
Con las nuevas recomendaciones de refuerzos Covid-19, las estimaciones sugieren que entre 100 y 200 millones de estadounidenses tendrán acceso a las vacunas de esta manera.
Estos cambios se hacen con el objetivo de basar las recomendaciones en la evidencia: simplemente no se sabe si una mujer sana de 52 años con un IMC normal, y que ha tenido Covid-19 3 veces, y que ha recibido 6 dosis previas de una vacuna Covid-19 se beneficiaría de la séptima dosis.
Esta política obligará a la generación de evidencia muy necesaria.
El Covid-19 no es una gripe
El Covid-19 se diferencia de la gripe en varios aspectos.
En primer lugar, el virus SARS-CoV-2 ha experimentado una evolución mutacional distinta a la de la gripe: la inmunidad inducida por la vacuna contra el Covid-19 podría no requerir actualizaciones anuales para obtener los resultados de salud más significativos desde el punto de vista clínico, pero podría desencadenarse por un cambio antigénico significativo.
En segundo lugar, el Covid-19 se transmite en verano, lo que puede facilitar la realización de estudios aleatorizados que se seguirán aplicando en el futuro.
En tercer lugar, la inmunidad natural al SARS-CoV-2 contra la enfermedad grave parece robusta.
En conclusión
La nueva filosofía de la FDA para el Covid-19 representa un equilibrio entre la flexibilidad regulatoria y el compromiso con la ciencia de referencia.
La FDA va a aprobar vacunas para personas de alto riesgo y, al mismo tiempo, va a exigir datos sólidos y de referencia sobre personas de bajo riesgo.
Estos ensayos clínicos van a orientar las futuras directrices de la FDA, basadas en la evidencia.
¿Y que va a pasar en Argentina?
Probablemente, en consonancia con estas nuevas recomendaciones, estas también sean adoptadas acá. En la actualidad, menos del 10 % de la población objetivo de Argentina recibió un refuerzo contra el SARS-CoV-2 el último año.
















